


1) コロナウイルス感染を防ぐ抗ウイルス薬の開発-
SARS-CoV-2の内核を構成するNタンパク質(NP)とゲノムRNAの相互作用を阻害する候補分子(TMP12)を見出し、ヒトコロナウイルスの増殖を阻害することを明らかにしました。現在、生体での効果を確認しさらに応用を目指して研究を行っています。
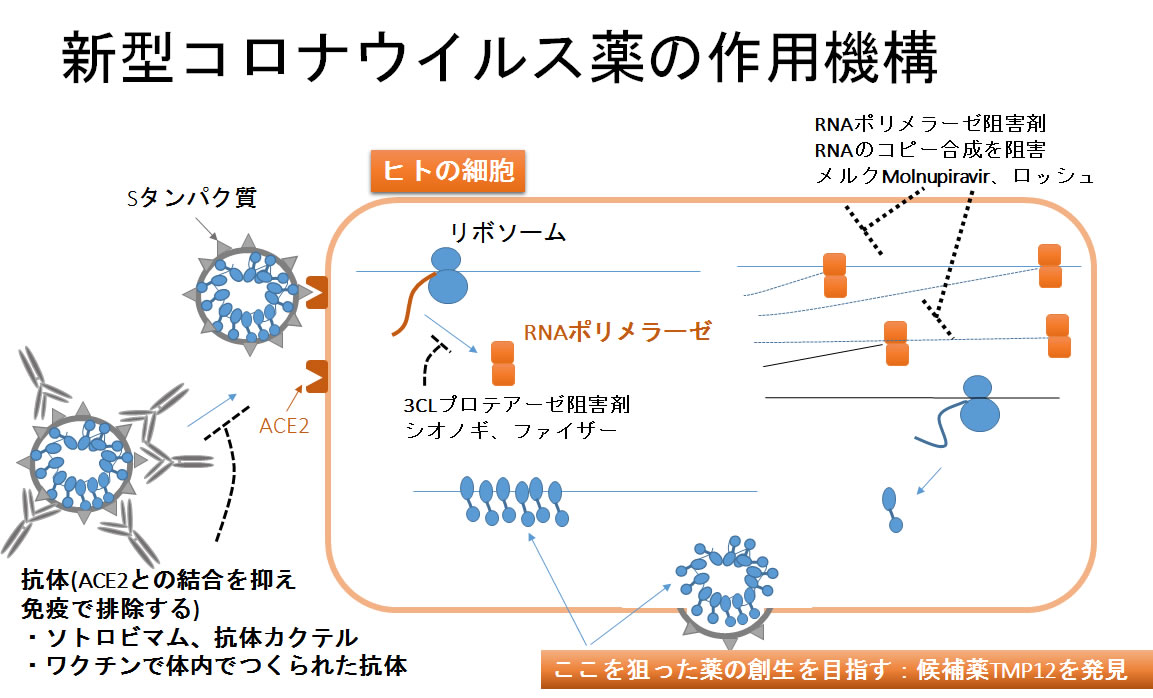
ソトロビマムなどの抗体医薬は、ウイルス表面のSタンパク質と結合してウイルス粒子を排除し、あるいはSタンパク質を介した細胞表面のACE2受容体への結合を阻害しその結果感染を抑えます。2021年10月現在、経口治療薬として治験が行われているのは、3CLプロテアーゼ阻害剤およびRNA依存性RNAポリメラーゼ(RNAのコピーを作る複製酵素)阻害剤です。私たちは、新しい作用点であるウイルス粒子の内核を構成するNタンパク質(NP)とゲノムRNAとの結合を阻害する分子(TMP12)を見出しました(下図)。
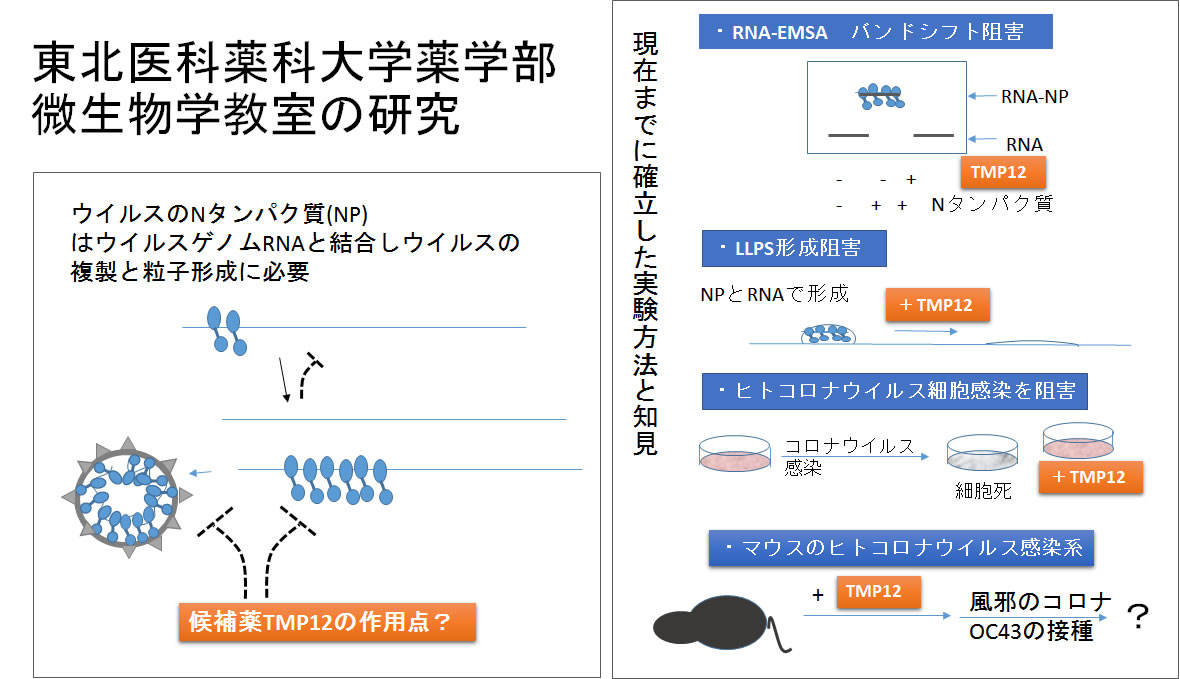
現在までに、TMP12は、NP-RNA相互作用、およびウイルス複製時のNP-ゲノムRNA相互作用を模倣した現象であるNP-RNAバイオコンデンセート形成(LLPS)を効率よく阻害する分子であることがわかりました。さらにTMP12はヒトコロナウイルスの細胞への感染をも抑制することを見出しました。現在、感染阻害効果の増強を検討しながらマウス感染モデル系を用いて検証することで、新たな方向性を持った治療法を提案するために研究を重ねています。
背景-21世紀に入り、約10年に一度の頻度で、重篤な呼吸器感染症のSARS、MERS、新型コロナウイルス感染症 (COVID-19)と立て続けに新たなコロナウイルス感染症が出現しました。人類が経験していないコロナウイルスが、動物の世界から漏れてきて新感染症が発生する可能性は示唆されてはいたもののCOVID-19の感染拡大を許してしまいました。COVID-19の病原体のSARS-CoV-2のゲノム情報から開発されたワクチンが広く接種され、ウイルス複製に必須な3CLプロテアーゼやRNAポリメラーゼを阻害する抗ウイルス薬の開発研究が進展、臨床試験が行われており、年内には承認されると予想されています。一方、今後危惧するのはウイルスの薬剤耐性化です。抗インフルエンザ薬は変異株を誘発することが分かっています。抗ウイルス薬物治療が成功に至っている後天性免疫不全ウイルス (HIV) やC型肝炎ウイルス (HCV) は、単一の薬物投与で出現する変異ウイルスに対応するため異なった作用点を持つ複数の薬剤を同時使用します。SARS-CoV-2のゲノムは、ヒトの免疫から逃避する方向、感染力が増大する方向に変異しており、今後使用される抗ウイルス薬が効きにくい変異ウイルスの出現の可能性があります。そこで、抗SARS-CoV-2薬の創出はもとより将来発生する「新コロナウイルス感染症」に対応する目的で、これまでにない発想でコロナウイルスのヌクレオキャプシドタンパク質 (NP) とウイルスゲノムRNAの相互作用を阻害する方法の開発を目指しています。
2) C型肝炎ウイルスコアタンパク質による細胞(小胞体)ストレス応答-
C型肝炎ウイルス(HCV)の病態の発現機構につながる研究です。 C型肝炎ウイルス(HCV)の日本における感染者は200万人、世界人口で3%とも言われています。感染後、数十年すると肝臓の障害、肝がんをおこし、実に、肝細胞がんによる死亡者の75%の原因となっています。近年、効率よくウイルスを駆除することができる薬剤が発売され高い治療効果を収めていますが、HCVが体内から駆除されても発がんのリスクは残ります。HCVはRNAウイルスで、がん遺伝子を持たないため、ウイルス感染による細胞の代謝変化が発がんにつながると考えられていますが、その発症機構を明らかにする必要があります。当研究室ではHCVコアタンパク質が小胞体の機能をかく乱し、脂質合成を誘導するなどHCVの病態の説明し得る現象を起こすことを明らかにしてきました。さらに、本学医学部との共同研究により肝がんを発症した患者から得られた変異HCV蛋白質が小胞体かく乱を増強することを明らかにし、これを抑制する化合物を東北大学の薬学研究科との共同研究で探索し候補物質を同定しました。現在そのメカニズムと効果に関して研究を進めています。
3) 酸化ストレスの感知細胞増殖の制御メカニズム-
私たちの体は、化学物質や紫外線、ウイルス感染など、様々なストレスに曝されています。このような刺激は細胞内で活性酸素を増加させ、この活性酸素は私たちの体を構成する細胞の蛋白質やDNAと反応して、様々な病気の発症に関与します。これまでにも活性酸素と病気に関する多くの研究がありますが、その感知機構のすべてが解明されたとはいえません。そこで、私たちは、細胞がどのように活性酸素を認識し、その情報を伝えるのか、分子メカニズムを探る研究を進め、活性酸素を受け取り活性酸素制御につなげる機構を明らかにし、この機構が、がん細胞の増殖に寄与することを明らかにしつつあります。現在、遺伝子改変マウスを用いて、抗がん剤の副作用発現メカニズムを解明する研究を行っています。この研究を進めることでがんや様々な病気を制御する方法の開発につながることを期待しています。