


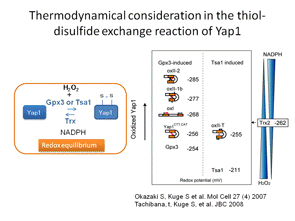
 図2.Yap1のレドックスポテンシャルの変化:クリックすると大きくなります。
図2.Yap1のレドックスポテンシャルの変化:クリックすると大きくなります。
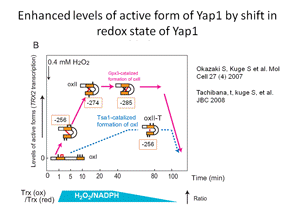 図3.Yap1が持続的に高い活性を維持する機構を初めて解明:クリックすると大きくなります。
図3.Yap1が持続的に高い活性を維持する機構を初めて解明:クリックすると大きくなります。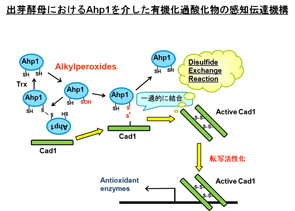
図4.ぺペルオキシレドキシンAhp1によるCad1転写因子の制御:クリックすると大きくなります。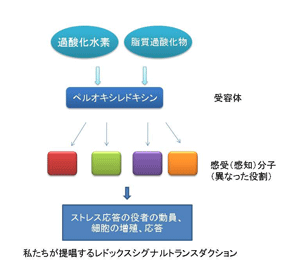 図5.ペルオキシレドキシンによるROS(過酸化水素)による感知と伝達。
図5.ペルオキシレドキシンによるROS(過酸化水素)による感知と伝達。
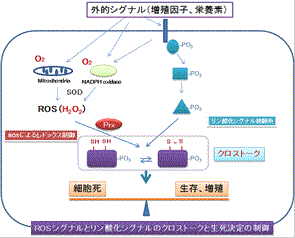 図6.ROSが決定する細胞の運命:クリックすると大きくなります。
図6.ROSが決定する細胞の運命:クリックすると大きくなります。
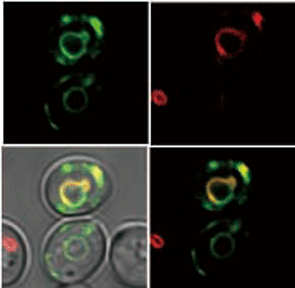 GFP融合Core蛋白質は小胞体表面に分布する。
GFP融合Core蛋白質は小胞体表面に分布する。

![]() Our research 4. C型肝炎ウイルスコアタンパク質の安定性制御機構
Our research 4. C型肝炎ウイルスコアタンパク質の安定性制御機構
![]() Our research 5. C型肝炎ウイルスコアタンパク質による小胞体ストレス誘導機構と毒性軽減を目指す創薬に関する研究
Our research 5. C型肝炎ウイルスコアタンパク質による小胞体ストレス誘導機構と毒性軽減を目指す創薬に関する研究
地球上の動物は呼吸をし酸素を利用して効率のよいエネルギーを作っています。 酸素は反応性に富み、電子の受け渡しを効率よく行うためこの性質を利用しているの です。 電子を受け取った酸素分子は最終的に水になりますが、その過程で発生する活性酸素は私たちの体を構成する細胞のタンパク質、脂質、DNAと反応してダメージを与え、様々 な病気の発症にも関係があることがわかってきました。
酸素の役割
反応性が高いので体にとって毒というお話をしましたが、酸素の毒性は体を外敵から守るためにも使われています。 ある種の免疫細胞は細菌などの外敵を食べて殺すことが知られていますが、免疫細胞内で殺菌するのにこの酸素の毒が使われているのです。また、最近の研究から、微量の活性酸素は正常な細胞の中で作られての細胞の活動をコントロールするシグナル分子として機能することもわかってきました。
体はどうやって酸素の毒性を防いでいるのでしょう?
私たちはこれまでに活性酸素種の一つである「過酸化水素」の 感知機構を明らかにしてきました。過酸化水素は活性酸素種の中で細胞内に比較的多く存在する分子です。その理由としては、酸素呼吸の過程等で主に発生する スーパーオキシドという活性酸素種は細胞質やミトコンドリアに多く存在するSODという酵素により過酸化水素に変換されること、また過酸化水素は比較的安 定であることなどが挙げられます。また、過酸化水素は膜透過性も高いため細胞外からも容易に細胞内に取り込まれ、細胞を構成するタンパク質、脂質、核酸を 酸化することでダメージを与えます。
では、過酸化水素はどのように細胞内で感知されているので しょうか?この問題に取り組むために、真核生物のモデルシステムとしてもっとも研究が進んでいる出芽酵母を用いて解析を進めてきました(酵母はあらゆる面 で貢献している生物ですね。パンやお酒を造るときに必要なパン酵母が基礎生命科学の進展にも貢献しています)。出芽酵母が過酸化水素等の毒性から身を守る ための立役者はYap1という転写因子です。過酸化水素があるときにYap1は形を変えて役者を動員する機能を果たします(図1)。そこで、私たちは過酸化水素の 存在がどのようにYap1を変えるかを研究すると一連の現象の本質が見えてくると考えて研究を進めてきました。その結果、ペルオキシレドキシンというタン パク質が過酸化水素のレセプターとして機能して(次の項目をみてください)、その情報(過酸化水素シグナル)をYap1やその他の分子に伝えていることが わかってきました。さらに、過酸化水素シグナルがYap1という主役に伝達される過程は酸化という反応ですが、それと同時に酸化された Yap1を元に戻す還元という反応もおきていることがわかりました。この酸化と還元は平衡状態であり、この平衡状態は酸化ストレス応答の過程で動的である がわかりました。この動的平衡状態が推移する過程で、Yap1は熱力学的な安定性を高める反応をおこすことで活性を維持(役者を動員する役割を)している ことを突き止めました(図2)。
なんだか難しい話に なってしまいました。私たちは実験結果をみて悩みながら、頭を柔らかく解釈する必要性を認識しこの結論に至りました。つまり、細胞内においては過酸化水素 により酸化される反応は同時に還元されているため可逆的です。その可逆反応は過酸化水素の濃度と細胞内の還元力(NADPH)の濃度で決定される平衡状態 におかれています。過酸化水素は徐々に減少します。一方、還元力は糖代謝反応により回復され維持されます。すなわち、酸化-還元の平衡状態は過酸化水素濃 度の変化に対応して推移していく状況が想定されます。過酸化水素がペルオキシレドキシンにより受容されそれシグナルとしてYap1に伝達する(活性化す る)過程は、Yap1分子内に存在する複数のシステイン(硫黄原子をもつアミノ酸の一つで酸化されることがある)の間で起こる酸化反応(ジスルフィド結合 形成)によって達成されることがわかりました。Yap1の酸化体はチオレドキシンという還元酵素(還元力NADPHに依存して)により還元されますので、見かけ上はYap1は一 定の酸化状態で止まっているように見えるますが実は酸化と還元が同時に起きた平衡状態に置かれています。最初にYap1におこる酸化(ジスルフィ ド結合)はすぐに還元されてしまいYap1が 立役者としての機能を全うできせん。そこでYap1は6つのシステインの間で3つの複数のジスルフィド結合を形成すると細胞内が元に戻るまで酸化型、すなわち活性型として量を維持する ことができるのです(図2、3)。
教科書には 「細胞の外や小胞体は酸化的な状態で細胞の中は還元状態であるので細胞質のタンパク質のシステインはジスルフィドを形成しない」という記述 を目にします。しかしながら私たちの研究は細胞質においても積極的にジスルフィド結合形成を誘導し、それを利用したシグナル伝達経路があることを示唆して おりますのでいずれ教科書の記述にも影響を与えると思います。
参考文献
1. 久下周佐「核外輸送のレドックス制御」 , 「バイオサイエンス の新世紀」「第5巻 酸化ストレス・レドックスの生化学」
日本生化学会編集 共立出版(2000)
2.
Kuge, S., M. Arita, A. Murayama, K. Maeta, S. Izawa, Y. Inoue, and A. Nomoto, Regulation of the yeast Yap1p nuclear export signal is mediated by redox signal-induced reversible disulfide bond formation. Mol Cell Biol, 2001. 21(18): p. 6139-50.
3.
Isoyama, T., A. Murayama, A. Nomoto, and S. Kuge, Nuclear import of the yeast AP-1-like transcription factor Yap1p is mediated by transport receptor Pse1p, and this import step is not affected by oxidative stress. J Biol Chem, 2001. 276(24): p. 21863-9.
4.
Kuge, S., T. Toda, N. Iizuka, and A. Nomoto, Crm1 (XpoI) dependent nuclear export of the budding yeast transcription factor yAP-1 is sensitive to oxidative stress. Genes Cells, 1998. 3(8): p. 521-32.
5.
Kuge, S., N. Jones, and A. Nomoto, Regulation of yAP-1 nuclear localization in response to oxidative stress. EMBO J, 1997. 16(7): p. 1710-20.
6.
Kuge, S. and N. Jones, YAP1 dependent activation of TRX2 is essential for the response of Saccharomyces cerevisiae to oxidative stress by hydroperoxides. EMBO J, 1994. 13(3): p. 655-64.
7.
Okazaki S, Tachibana T, Naganuma A, Mano N, Kuge S. Multistep disulfide bond formation in Yap1 is required for sensing and transduction of H2O2 stress signal.
Mol Cell. 2007 Aug 17;27(4):675-88
ここでは、タンパク質の中にあるシステインどうしの間に 可逆的なジスルフィド結合を起こすことで過酸化水素シグナルを受容し伝達する現象をレドックスシグナル伝達と呼ぶことにします。上述の研究は出芽酵母 Yap1がその補助因子としてGpx3というタンパク質が働いていることを示したToledanoらの研究を基盤としています。Gpx3はグルタチオンペ ルオキシダーゼに類似な分子として同定されましたが意外にもペルオキシレドキシン活性を持っております。彼らがこの現象を報告をした頃、私たちも、主要ペ ルオキシレドキシンであるTsa1(細胞内のペルオキシレドキシンの94%をしめる)が、Gpx3と同様にYap1の酸化を促進することを試験管内の実験 から明らかにしていました。実際にTsa1にも過酸化水素受容体としての機能はあるのでしょうか?私たちはこの可能性を追求すべく研究を進 めた結果、どうも答えはYesの様です。
これまでに、特定の実験室酵母株ではYap1に過酸化水 素シグナルを伝達しているのはGpx3ではなくTsa1であること、Tsa1はYap1に過酸化水素シグナルを伝えるが完全でないために立役者Yap1の 活躍も不十分であることを明らかにしました。これらの結果は、主要ペルオキシレドキシンであるTsa1も過酸化水素受容体として機能することを示唆してい ます。また、最近Tsa1にはYap1以外の本質的なターゲット因子、すなわち過酸化水素シグナルを受け渡す相手が存在することを明らかにしました。 Tsa1のようなペルオキシレドキシンは過酸化水素と反応して水に還元するペルオキシダーゼと考えられてきましたが、私たちの研究は、ペルオキシレドキシ ンは過酸化水素のレセプターとして機能することを示しています。ペルオキシレドキシンの本質的な機能はこちらかもしれません。
ところでペルオキシレドキシンには5つの類似分子が存在し ます。そこで疑問です。Tsa1以外のペルオキシレドキシンにも同様に過酸化水素受容体の活性があるのでしょうか?私たちは少し異なった構 造をしたペルオキシレドキシンのAhp1が有機過酸化物質レセプターとして機能することを明らかにしました。Ahp1は過酸化物質から受け取ったシグナルをCad1転写因子に伝達して抗酸化蛋白質やシャペロン遺伝子の誘導に寄与することが分かりました。この場合もCad1分子内のジスルフィド結合形成が活性化につながっています(図4)。私たちが提唱してする概念がここでも裏付けられました(図5)。
8. Okazaki, S. Naganuma A. and Kuge S. Peroxiredoxin-mediated redox regulation of the nuclear localization of Yap1, a transcription factor in budding yeast. Antioxid Redox Signal. 3-4, 327-334 (2005)
9. Tachibana T, Okazaki S, Murayama A, Naganuma A, Nomoto A, Kuge S. A major peroxiredoxin-induced activation of Yap1 transcription factor is mediated by reduction-sensitive disulfide bonds and reveals a low level of transcriptional activation. J Biol Chem. 2009 Feb 13;284(7):4464-72. Epub 2008 Dec 22.
10. Iwai, K, Naganuma, A and Kuge S. Peroxiredoxin Ahp1 acts as a receptor for alkylhydroperoxides to induce disulfide bond formation in the Cad1 transcription factor. J Biol Chem. 2010 Apr 2;285(14):10597-604. Epub 2010 Feb 9 2010.
上述の研究はモデル真核生物として出芽酵母を用いて新たな 概念を提唱する研究です。ところでヒトの細胞においても同様な機構が存在するのでしょうか?ヒトなどの哺乳動物細胞においても酸化ストレスが様々な病態の 原因となっていることが示されております。また、ヒト細胞が増殖因子に応答したときに細胞内で活性酸素種が作られそれが増殖因子の情報を細胞内で伝えるた めに重要な役割を果たします。これら事実は細胞が過酸化水素などの活性酸素を認識してそれをストレスとして感じる場合と増殖のシグナルとして感じる場合が あることを示しています。そこで受容体とそのシグナルの伝達機構、すなわちレドックスシグナル伝達を理解することが大切です。私たちはヒト細胞のペルオキ シレドキシンが過酸化水素の受容体として機能しその情報を他の分子に伝達する可能性を追求しています。前述したように、哺乳動物細胞の場合はレドックスシ グナル伝達により細胞を増殖させる方向性に導くか、過度の酸化ストレス状態では積極的に細胞死を選択する場合もあると考えられます。従って、ペルオキシレ ドキシンを受容体としたレドックスシグナル伝達とそれによる制御機構は「細胞の運命決定」の中心的役割を演じている可能性があります(図6)。
日本にはC型肝炎ウイルス(HCV)の感染者は200万人ともいわれています。HCVは 持続的に感染し、数十年たつと肝硬変、肝細胞癌になる確率が高くなる。HCV感染者からのウイルス の駆除または肝細胞癌発症の抑制を目指した治療法の開発と改善が行われていますが、現存の治療法が適用できない場合があり新たな治療法の開発も期待されて います。私たちは、HCVのウイルス粒子を構成する蛋白質の1つコア蛋白質が出芽酵母の増殖を阻害 することを見いだし、HCVコア蛋白質による増殖阻害を解除する核内輸送阻害を解除する薬剤の酵母 を用いたスクリーニング系の構築を行い、実際に、北里研究所(大学)供田先生との共同研究で抗生物質ライブラリー等のスクリーニングを実施いたしました。
ところで、C型肝炎ウイルスは持続感染し数十年をかけて肝が んを発症しますがそのメカニズムは明らかにされておりません。C型肝炎ウイルスはRNAをウイルス遺伝子として持つウイルスでがん遺伝子を持ちませんし、 ウイルスの増殖は細胞質で起こりますのでウイルスの複製過程で核に存在する遺伝子DNAに傷をつけて発がんにつなげるのではなく、ウイルス複製の過程でお こる代謝の変化により出される活性酸素種が長い時間をかけてDNAに傷をつけて発がんにつなげると予想されされています。この点で興味深いのがウイルス粒 子の構成分子であるコアタンパク質が引き起こす現象です。コアタンパク質を肝臓細胞に作らせるとそれだけで活性酸素種が増加したり、マウスの肝臓に発現さ せた場合は長い期間を経て肝がんを起こすことなどが報告されています。
そこで私たちはコアタンパク質により引き起こされる代謝 変化に着目して研究しています。しかし問題があります。長い間かけて起こす代謝変化を研究するのは大変ですし、その現象を理解するための役 者を見いだすのが難しいと考えました。そこでまた酵母細胞が登場です。私たちはこれまでに、酵母細胞にコアタンパク質を発現させると小胞体ストレスを起こ すことを見いだしています。小胞体はその内部でたくさんのタンパク質を合成します。小胞体内で合成されたタンパク質は厳密な品質管理かに置かれ、良い品質 のものが小胞輸送という方法で細胞内外の目的地に運ばれます。小胞体内部でタンパク質が質的に低下するそれを感知して、そのタンパク質を修復したり、分解 したりすための役者を揃える機構が小胞体ストレス応答です。コアタンパク質を酵母細胞に発現させると小胞体の周りに集まります。小胞体の周りに集まるコア がなぜ小胞体内部のタンパク質の品質管理機構に影響を与えるのでしょうか?私たちは、このちぐはぐとも思える現象が細胞の恒常性変化(ヒトの肝臓細胞では 病態)につなが可能性があるのではと考えています。そこで、なぜコアタンパク質が小胞体ストレス応答を作動させるのか、また、その結果おこる恒常性の変化 とその原因は何かを研究しています。きっと、酵母がヒトのモデルとなって役に立ってくれると期待しています。