NEWS
LATEST NEWS
LATEST NEWS
・コアフコース糖鎖が減少すると脳の免疫系を担うミクログリアの過剰な活性化が引き起こされるが、L-フコースの経口投与により脳内のコアフコース糖鎖が増加し、ミクログリアの活性化が抑制された。
・コアフコース糖鎖が減少するとIL-6受容体の複合体形成が促進し、炎症反応が活性化する。しかし、L-フコースの投与により複合体形成が抑制された。
・L-フコースによる神経炎症の抑制は、精神疾患等に対する予防・治療法の分子基盤となる可能性がある。
東北医科薬科大学 薬学部の顧建国 教授、山口芳樹 教授、医学部の森口尚 教授、広島大学大学院 統合生命科学研究科 中ノ三弥子 准教授らの研究グループは、糖転移酵素のひとつであるFut8による神経炎症抑制とその仕組みを明らかにしました。また、広く生物界に分布している糖の一種であるL-フコースが神経炎症抑制化合物であることを明らかにしました。
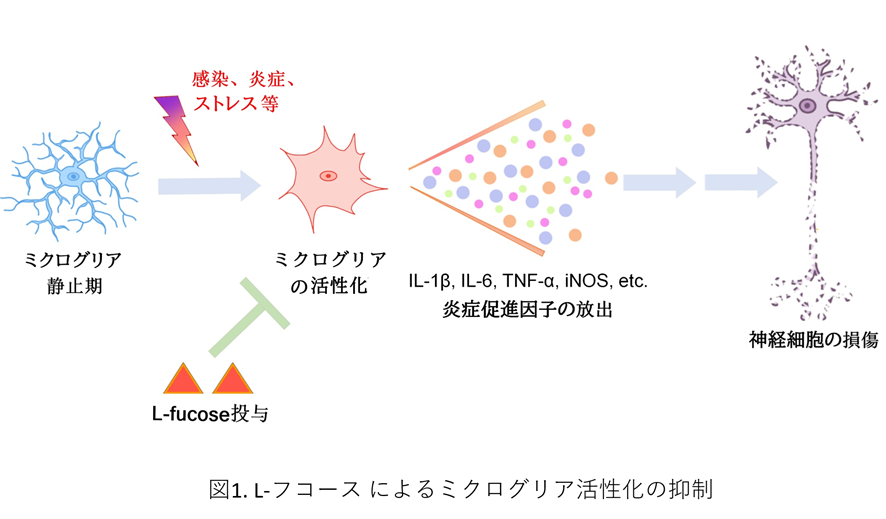
糖鎖修飾は最も一般的な翻訳後修飾で、複雑で多様な構造をとる糖鎖1はさまざまな受容体の機能調節に働いていることが知られています。その中で、コアフコース糖鎖2は糖転移酵素Fut8によってフコースがN-結合型糖鎖1の根元に付加される構造です。脳はFut8が最も高発現する組織です。本研究では、図1のように脳内の免疫を担当するミクログリア3の活性化がL-フコースの投与によって抑制されることと、その制御メカニズムを解明しました。さらに、コアフコース糖鎖を生体に負荷をかけずに増加させることが出来ることを明らかにしました。この研究結果は、神経炎症が関連した疾患の新しい予防・治療戦略につながることが期待されます。なお、この研究成果は米国の科学雑誌The Journal of Biological Chemistry (JBC)に2023年11月30日付で公開されました。
(用語解説)
*1. 糖鎖・N-結合型糖鎖: 単糖が鎖のようにつながったもので、たんぱく質や脂質と結合して細胞の表面細胞の表面を覆っています。糖鎖がタンパク質に結合する様式は2通りありますが、アスパラギンの側鎖に結合するのがN-結合型糖鎖です。N-結合型糖鎖は様々な膜受容体の機能を調節しています。
*2. Fut8・コアフコース糖鎖:コアフコース糖鎖はさまざまなN-結合型糖鎖の還元末端にフコースを持つ糖鎖です。哺乳動物においては、コアフコース糖鎖はα1,6フコースだけを指し、付加できるのはフコース転移酵素の中でもFut8だけです。コアフコース糖鎖には様々な生理活性がありますが、がん・炎症と最も関係が深い糖鎖修飾の1つです。
*3. ミクログリア:グリア細胞の一つで、免疫を担当する細胞です。正常状態では点在していますが、炎症が生じると、細胞体の肥大化や細胞増殖を伴い活性化状態となり、炎症性サイトカインの産生放出を引き起こします。
 詳細はプレスリリース本文をご確認ください。
詳細はプレスリリース本文をご確認ください。
Exogenous L-fucose attenuates neuroinflammation induced by lipopolysaccharide
掲載紙:The Journal of Biological Chemistry (JBC)
ウェブサイト:https://www.sciencedirect.com/science/article/pii/S0021925823025413?via%3Dihub
著 者:Xing Xu1; Tomohiko Fukuda1; Jun Takai2; Sayaka Morii3; Yuhan Sun1; Jianwei Liu1; Shiho Ohno4; Tomoya Isaji1; Yoshiki Yamaguchi4; Miyako Nakano3; Takashi Moriguchi2; Jianguo Gu1
著者所属:1東北医薬大・分生研・細胞制御; 2東北医薬大・医・医化学; 3広大院・統合生命科学; 4東北医薬大・分生研・糖鎖構造生物学
分子生体膜研究所(所長 顧建国 教授)
薬学部/細胞制御学(責任者 顧建国 教授)
薬学部/糖鎖構造生物学(責任者 山口芳樹 教授)
医学部/医科学(責任者 森口尚 教授)